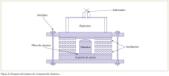
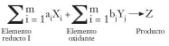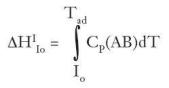La técnica SHS para síntesis y fabricación de materiales cerámicos
Fundamentos teóricos, ventajas e inconvenientes, y aplicaciones industriales de la técnica de síntesis de materiales por combustión (SHS o Self-propagating High-temperature Sintesis)
Introducción
Uno de los principales campos de estudio en la ciencia y la ingeniería de los materiales se encuentra en los materiales cerámicos. En los últimos tiempos se han llevado a cabo estudios sobre la mejora de propiedades obteniéndose importantes avances. Entre los prin cipales inconvenientes se encuentra su elevado coste de producción debido a su proceso de síntesis, ya que se trata de materiales que requieren diferentes eta-pas: conformado, densificación y acabado. En este aspecto se está trabajando para intentar reducir los costes sin men-guar las propiedades del material,. Una de las opciones que se está barajando actualmente es la técnica SHS.
Fundamento teórico
La técnica SHS (Self-propagating High-temperature Síntesis) consiste en la obtención de diferentes materiales con mínimos aportes energéticos y sin necesidad de aplicar altas temperaturas. El ahorro energético que se establece en este proceso proporciona un hecho importante para su estudio, debido al gran avance que supone en el proceso productivo.
Dicha técnica, también conocida con el nombre de síntesis de materiales por combustión, está basada en las reacciones químicas que se producen cuando se mezcla un sólido con sólido o sólido con gas. En las reacciones sólido -sólido el mecanismo queda regido por mecanismos de difusión, mientras que para las reacciones sólido-gas la relación de superficies adquiere una relevante importancia.
Las reacciones establecidas son fuertemente exotérmicas, es decir, que el calor desprendido de la masa reaccionante permite su autopropagación mediante una onda o frente de combustión. En la técnica SHS se pueden considerar dos tipos de procesos:
1. Propagación de onda, donde la reacción se inicia en una parte de la muestra, creándose un frente de combustión que se desplaza a lo largo de la misma. La temperatura de dicho frente, dependiendo de los procesos, puede alcanzar hasta 4.000 ºC, desarrollándose en algunos de ellos presiones de hasta 2.500 Pa. La propagación de una onda de combustión depende fuertemente de la conductividad térmica del sistema y de la energía de activación de la reacción química.
2. Explosión térmica en donde la reacción se inicia simultáneamente en todo el volumen de la muestra al alcanzarse la temperatura de ignición.
La onda de propagación puede desplazarse a través de la muestra de diferentes formas y según su propagación se pueden establecer dos tipos de reacción:
1. según un modo estable, en cuyo caso la velocidad del frente de combustión es constante a lo largo de la reacción o, lo que es lo mismo, el desplazamiento del frente es uniforme con el tiempo y,
1. según un modo inestable en cuyo caso la velocidad del frente de combustión no puede considerarse constante. Dentro de este tipo de reacción se pueden distinguir fundamentalmente dos casos:
– velocidad oscilante donde el desplazamiento del frente se produce de forma no uniforme con el tiempo
– velocidad espinodal donde la reacción se produce con un movimiento espiral desde un extremo a otro de la muestra.
De cualquier manera, se produce una onda o frente de combustión con una determinada velocidad que viaja a través de los reactivos convirtiéndolos en el producto deseado. Se puede escribir como ecuación general de reacción SHS la siguiente:
donde: X = Ti, Zr, Hf, V, Nb, Ta, etc.
Y = B (Z = boruros), C (Z = carburos), N (Z = nitruros), etc.
La reacción es muy similar a la de un proceso de combustión convencional.
En definitiva un proceso SHS es una reacción química iniciada gracias a un aporte de energía, a partir del cual se autopropaga la reacción. Para que una reacción sea autosostenida debe ser altamente exotérmica y ello está asociado a elevadas temperaturas. Un parámetro de gran utilidad que proporciona una buena aproximación de la temperatura alcanzada por el producto durante la reacción es la temperatura adiabática de combustión Tad.
La temperatura adiabática de combustión se define como aquella que alcanzarían los productos de la reacción, en condiciones adiabáticas, como consecuencia de la energía producida por la reacción química. La Tad puede calcularse suponiendo que la entalpía de la reacción va dirigida únicamente a elevar la temperatura de los productos y, por tanto, no existen pérdidas con el exterior, es decir, suponiendo un sistema cerrado.
Así, considerando la reacción:
ATo+ BTo? ABTo+ ?Hr,To
donde:
Aunque las reacciones SHS se caracterizan en ocasiones por su Tad, es preciso delimitar su significado, pues se trata únicamente de una medida de la exotermicidad de la reacción y define el límite superior de temperatura para un sistema de combustión determinado. Algunos autores han sugerido un criterio empírico según el cual si Tad < 1.800 K la combustión autosostenida no tiene lugar y si Tad > 2.500 K la combustión SHS se produce. En el rango 1800 K < Tad < 2.500 K, la onda de combustión no se propaga por sí misma, pero es posible que la combustión se produzca ayudada por técnicas adicionales como el precalentamiento de los reactivos.
Otros factores a tener en cuenta son la densidad y la conductividad térmica sobre todo en aquellos reactivos que presentan una elevada conductividad, o bien cuando la densidad de los compactos es alta.
Ensayos experimentales
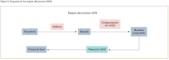
La base del proceso SHS es la utilización de reacciones químicas exotérmicas que producen una onda de combustión que se transmite a través de los reactivos de la muestra convirtiéndolos en los productos deseados. En la reacción de combustión que tiene lugar hay dos factores importantes que entran en juego: por un lado la velocidad de propagación del frente y la temperatura de combustión.
La primera etapa del proceso SHS consiste en mezclar polvos de tamaños y composiciones diferentes, en ocasiones se añaden aditivos que actúan como lubricantes durante el compactado o aglutinantes que incrementan la resistencia del compactado crudo. El polvo suelto se comprime a través de prensas mecánicas o hidráulicas en una matriz, resultando una forma que se conoce como pieza en verde o compactado crudo. Las prensas utilizadas en este procedimiento generalmente son uniaxiales, en la que la presión se aplica al polvo en una sola dirección con el objetivo de obtener piezas con acabados precisos.
La técnica SHS ha sido objeto de gran atención como método alternativo para fabricar materiales cerámicos debido a que esta técnica presenta un bajo coste respecto a los procedimientos que se emplean actualmente para la síntesis de materiales cerámicos. Para la síntesis de materiales cerámicos se parten de polvos cerámicos, a través de una reacción autopropagada después de un inicio local de la misma. En la reacción típica de síntesis por combustión los reactivos mezclados (en polvo) se presionan para formar bolas de una cierta densidad. A continuación se llevan a la temperatura de ignición local-mente en un punto, o bien calentando toda la bola (modo de combustión simultánea), produciéndose una reacción fuertemente exotérmica que da lugar a la síntesis del material.
La temperatura de ignición es un parámetro importante en una reacción SHS y se define como la temperatura a partir de la cual el flujo de energía generado en la propia reacción química sobrepasa las pérdidas por radiación, convección y conducción, alcanzándose el régimen de autocombustión.
Para alcanzar la temperatura de ignición se precisa una fuente externa de energía que deberá cumplir dos requisitos fundamentales:
1. Debe elevar la temperatura de la mezcla hasta la temperatura de ignición.
2. Debe realizar un aporte energético lo bastante rápido para evitar que un porcentaje significativo de la energía generada se pierda por intercambio con el medio, de forma que no se alcanzaría la temperatura de ignición.
La búsqueda de producción de materiales densos mediante SHS sugirió la presencia de una fase líquida durante la reacción que permitiera la densificación del producto a través de la aplicación de presión. En este campo existen algunas variantes tales como la compactación dinámica, prensado axial (comentado anteriormente) o el prensado isostático (compactación aplicando una presión hidrostática mediante un fluido que puede ser agua o aceite). En la compactación dinámica (CD) la muestra se somete a elevada presión, una vez terminada la reacción SHS. El material poroso resultante de la reacción SHS se densifica por la acción de una onda de presión, generada por una detonación activada inmediatamente después de la reacción.
Ventajas e inconvenientes
Entre las principales ventajas que presenta la técnica SHS respecto a otros métodos convencionales de procesamiento de cerámicos cabe destacar:
1. La alta temperatura de la reacción puede volatilizar las impurezas de bajo punto de evaporación y, por consiguiente, se obtiene un producto final de alta pureza.
2. La naturaleza exotérmica de la reacción SHS supone un ahorro económico por la facilidad del proceso y del equipamiento necesario.
3. El tiempo de reacción es relativamente corto y hace que los costes de procesamiento y operación sean relativamente bajos.
4. El producto final puede ser sin tetizado y consolidado en un solo paso, utilizando la energía química de los reactivos.
Además de los aspectos comentados anteriormente, cabe destacar el bajo requerimiento energético, la simplicidad y sencillez del equipamiento necesario y la alta productividad debido a las rápidas velocidades de reacción.
Por el contrario, el principal problema cuando se desea obtener piezas densas es la alta porosidad de los compactos obtenidos (del orden del 50%). Las fuentes de esta porosidad no deseable en la mayoría de los casos son:
1. Poros en la mezcla de reactivos, que a su vez producen poros en el producto, ya que hay poco tiempo para su eliminación.
2. Volatilización de las impurezas durante la reacción a alta temperatura y eliminación de los gases generados en superficie.
3. A menudo la densidad cristalográfica de los productos es mayor que la de los reactivos.
4. Expansión de los gases ocluidos en el interior de la muestra.
Para evitar la formación de la porosidad, una posible solución es la aplicación de un grado suficiente de presión durante el proceso de síntesis.
Aplicaciones industriales
Entre los diferentes materiales que se pueden obtener a través de la técnica SHS cabe destacar los silicuros (MoSi2), óxidos (Al2O3, ZrO2, TiO2), aluminuros (TiAl3, NiAl, Ni3Al, FeAl), boruros (TiB2, MgB2, TiC – TiB2), carburos (WC, TiC, SiC), nitruros y metales tales como Cu, Ti, Fe, Mo. La técnica SHS es utilizada en muy diversos campos, desde obtención de materias primas hasta conformado de piezas complejas, desde materiales simples hasta materiales compuestos con función gradiente.
Respecto a las aplicaciones de la técnica SHS, presenta un auge importante en el sector petroquímico (catalizadores, cementos refractarios, recubrimientos), sector cementero (recubrimientos en placas para antidesgaste y sometidos a altas temperaturas), sector metalúrgico (afinadores de grano, obtención de ferroaleaciones), sector biomédico (empastes dentales, prótesis de materiales avanzados como NiTi), tratamientos superficiales, bienes de equipo y en la obtención de piezas abrasivas a partir de residuos metálicos entre otros.
Bibliografía
Ceramic Application & Design, Ceramic Industry, Corcoran Publ., USA, February 1988, pp. S3.
Merzhanov A.G. (1991), in Combustion Process in Chemical Technology and Metallurgy, ed. A.G. Merzhanov, Chernogolovka, Rusia.
Merzhanov A.G. (1993), “Combustion processes that synthesize materials”, Keynote lecture presented at the AMPT’93 International Conference, Dublin, Ireland, (1993).
J.S. Moya, C. Baudín, P. Miranzo, (1992). En Enciclopedia of Physical Science and Technology, 5, Academia Press Inc. 2ª edición, USA.
W.D. Kingery, K.H. Bowen, D.R. Uhlmann, (1986). Introduction to Ceramics, 2ªedición, John Wiley and Son, New York, USA.
RESUMEN
La técnica SHS (Self-propagating High-temperature Síntesis) constituye un novedoso avance en los métodos de síntesis y fabricación de materiales de tipo cerámico, que se basa en la utilización del calor generado en reacciones químicas exotérmicas, y que representa un importante ahorro energético, además de reducir los costes de las correspondientes instalaciones térmicas. En este artículo se explican los modelos y mecanismos teóricos en que se basa el proceso SHS, para luego considerar las ventajas e inconvenientes de su aplicación práctica. Por último, se hace especial hincapié en las ventajas de ahorro energético que representa la aplicación industrial de esta técnica