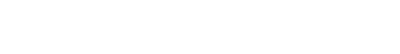La inducción en procesos de ionización

Ciertas ondas electromagnéticas asociadas a un campo eléctrico aumentan la movilidad iónica en un proceso electrolítico
El objetivo de este trabajo es hacer un estudio del aspecto físico de un proceso electrolítico y la influencia que pueden tener las ondas electromagnéticas.
Conductores
Son buenos conductores los cuerpos que dejan pasar a su través la electricidad; en general son buenos los metales, denominados de primera clase, para distinguirlos de otros compuestos que disueltos en agua u otros disolventes se hacen conductores y que se denominan de segunda clase.
En el primer caso, lo que se desplaza son los electrones, llamados libres y que se encuentran en la última capa atómica; en el segundo, lo que se desplaza son moléculas o partículas atómicas cargadas eléctricamente.
Por último, hay otro tipo de conducción debido a la ionización de ciertos gases (generalmente) a determinadas condiciones de presión y temperatura, como consecuencia de que ciertas radiaciones arrancan electrones de las últimas capas.
Electroquímica
Es la parte de la física-química que estudia las reacciones químicas que se producen al paso de una corriente eléctrica; y las corrientes eléctricas generadas al reaccionar ciertos compuestos químicos.
Como se sabe, ciertos compuestos o sustancias al disolverse en el agua se ionizan; si introducimos dos conductores metálicos e inertes, unidos a un generador de corriente continua se produce una reacción química. El proceso químico producido por la corriente eléctrica se llama electrolisis; el recipiente que contiene la disolución y los conductores, celda o cuba electrolítica; electrolito, la sustancia disuelta; el conductor unido al polo positivo, ánodo; el conductor unido al polo negativo, cátodo; los iones que se dirigen al polo positivo y cargados negativamente, aniones; y los iones que se dirigen al polo negativo, cargados positivamente, cationes.
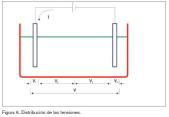
Aplicación de una tensión continua a una cuba electrolítica
Sea una cuba electrolítica formada por un recipiente de vidrio, dos electrodos de platino, separados unos cuatro centímetros, y el electrolito H2SO4, 0,5 M.
Si se aplica progresivamente una tensión entre 0-4 voltios se observa que hasta los 2,2 voltios no circula corriente por el denominado efecto de la doble capa que se produce en cada electrodo (entre el metal y el electrolito). Al valor de la tensión donde empieza a circular corriente se denomina fuerza contraelectromotriz y es igual o superior a la suma de los potenciales de cada electrodo.
Se va aumentando la tensión y se produce una corriente, como consecuencia de la movilidad de los iones; la movilidad total será la suma de las movilidades de los aniones y cationes. Si definimos v+ como la movilidad de los cationes y v-la movilidad de los aniones, la movilidad total es: v = v+ + v-
La conductividad c = c+ + c- (Relacionadas con la movilidad por el faradio)
Y las resistencias c+ = 1 / R1; c- = 1 / R2; c = 1 / R
Por lo tanto 1/R = 1/ R1 + 1 / R2
Al aumentar la tensión aumenta la intensidad en mayor proporción, por lo tanto la resistencia no es constante.
Magnetismo creado por una carga (un ion) en movimiento
Una carga eléctrica en movimiento produce en su proximidad un campo magnético; lo enunció en 1820 el físico danés Hans Christian Oersted.
Las líneas de fuerza son circunferencias situadas en el plano perpendicular al vector velocidad, cuyo centro está en el trayecto y cuyo sentido es el de giro del sacacorchos que avanza con la carga si ésta es de signo positivo y sentido contrario si es negativa, la dirección del campo magnético es perpendicular tanto a la dirección del movimiento como a la dirección de la línea que une el punto más cercano del trazado con el punto, y su valor vale:
DB =(µ0/4p)x dqvn/r “Ley de Biot y Savart” B = K qv/r2
K = µ0 / 4 p
µ0 = 4p × 10-7
K = 10-7
r, metros
v, metros / segundos
q, culombio
B, weber / metro cuadrado = tesla = T
K = 10-7Wb / A. m
1 T = 104 gaus
En la sección transversal de la cuba se observa que a un ion rodeado de iones de signo contrario, le llegan las líneas de fuerza del campo magnético y cuya suma vectorial es cero; sin embargo, si observamos la cuba en sentido longitudinal apreciamos que cada ion origina un campo magnético debido al movimiento de los iones y que es del mismo sentido y dirección pero de valor variable en cada punto dependiendo de la posición de la carga.
Es interesante conocer el valor del campo magnético, que se consigue hallando el coeficiente de autoinducción.
Este valor se puede obtener considerando que una cuba electrolítica es un circuito RL; aplicando una tensión continua y observar la respuesta de la intensidad: midiendo la constante del circuito.
Otra forma es pensar que está formada por una infinidad de líneas, tantas como iones existen transversalmente en una cuba electrolítica y hallar su valor. Para una disolución NaCl ; 0,5 M, disposición centrada en la cara del cuadrado y distancia 7,49 Aº, siendo el radio atómico del Cl- de 1,81 Aº y el radio del Na+ de 0,95 Aº la autoinducción obtenida es de 0,312 × 10-9 henrios /cm.
L = 2 × 10-7 Dm / Ds
Siendo Dm la distancia media geométrica entre iones de distinto signo y
Ds la distancia media geométrica entre iones del mismo signo.
Tensión inducida creada en una cuba electrolítica
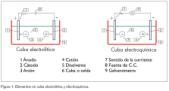
Aplicando la regla del sacacorchos o de la mano derecha, para los iones de signo positivo, el dedo índice nos indica la dirección del movimiento y los demás dedos la dirección del campo magnético; en la figura 2 el punto (·) indica que el campo magnético salen del papel y la cruz x que entran. Para las cargas negativas, se mueven en sentido contrario, la dirección del campo magnético es la misma.
Sea un ion cargado positivamente; el tiempo que tarda en pasar junto a dos iones negativos consecutivos viene dado por:
t1 = l1 / (v1 + v2)
Siendo l1 la separación entre dos iones negativos consecutivos
v1 la velocidad de los iones positivos
v2 la velocidad de los iones negativos
Lo mismo para cada uno de los iones negativos
t2 = l2 / (v1 + v2)
Si se supone que están distribuidos de forma uniforme en la disolución todos los iones
Siendo la frecuencia f1 = 1 / t1
f2 = 1 / t 2
Se obtiene
f1 = (v1 + v2) / l1
f2 = (v1 + v2) / l2
La longitud o separación entre iones depende de la concentración de la disolución
En sus movimientos los iones cortan las líneas de fuerza del campo magnético creando una fuerza electromotriz independiente del signo de su carga y cuya polaridad en cada ion sólo depende del sentido de su movimiento. Los iones no se pueden desplazar en sentido perpendicular a su trayectoria porque se lo impiden los de signo contrario. Pero se crea un desplazamiento de cargas que, como se aprecia en la figura 3, crea fuerza de repulsión entre iones de distinta carga que facilita el movimiento de los mismos; de aquí se desprende que aumente la intensidad en mayor proporción al aumentar la tensión entre los electrodos. En el efecto Hall, se desplazan las cargas en sentido transversal a su movimiento, bien sean iones o electrones, creando una pequeña intensidad de campo debida a la Fem. producida; en este caso se lo impiden los iones que circulan en sentido contrario y lo que ocasiona es que iones de signo distinto se repelen.
Se ha indicado que el campo magnético de la disolución es la suma de cada uno de los campos que produce cada ion y que genera una Fem. pero difícil de calcular su valor; podemos considerar como el formado por dos haces de conductores juntos entre sí y que circula por cada uno de ellos una intensidad I
Y donde B = k · 2 · I / d
Y con una variación de B con una frecuencia f (valores muy pequeños debido a que la velocidad de los iones es pequeña).
Por otra parte, una carga eléctrica experimenta una fuerza cuando se mueve en un campo magnético. Esta fuerza llamada magnética y que ejerce el campo magnético sobre la carga en movimiento es: F = B · q · v
De aquí que conductores por los que circulan corrientes de distinto sentido se atraen.
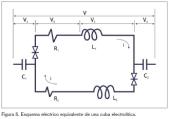
Hagamos la siguiente experiencia: apliquemos a un haz de conductores aislados y próximos entre sí una forma de onda puntual e instantánea de un valor I con una frecuencia determinada. Este haz a su vez está entrelazado con otro.
Comprobar la Fem. autoinducida en el mismo haz y la Fem. inducida en el otro.
Estudiar el coeficiente de autoinducción y de inducción mutua del circuito.
Aplicar en sentido contrario una onda puntual e instantánea de la misma amplitud pero de valor negativo.
Hay que hacer la observación de que la resistencia de una cuba electrolítica es mucho más elevada que la resistencia de cada haz de conductores.
En el caso de la electrolisis el campo magnético varía con respecto al espacio y en esta experiencia varía con respecto al tiempo.
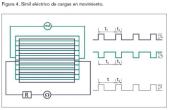
Circuito eléctrico
Se representa el esquema eléctrico a tenor de lo expuesto anteriormente. (Me he tomado la licencia de colocar diodos en oposición para indicar que hay dos corrientes iguales y opuestas).
Aplicación de un campo magnético a una cuba electrolítica
Hasta ahora se ha estudiado que los iones en su movimiento crean un campo magnético y que además se produce una Fem. si se cortan las líneas de dicho campo magnético. La intensidad de campo creado por cada carga eléctrica es muy pequeña, aunque la distancia a la carga sea pequeña; lo mismo ocurre con la Fem. debido en ambos casos a que influye la velocidad y ésta es muy pequeña en los casos que estamos tratando.
Por ello, consideremos un ion dentro de un campo magnético producido por el mismo o exteriormente.
Vamos a generalizar la Ley de Neuman y Lenz
Fem. = -d?m / dt = -d (B · a · cosa) / dt
Aplicando la regla para diferenciación de un producto
Fem. = – a · cos adB / dt – B cos ada / dt + B · a sen ad0 / dt
El primer término depende de la variación del módulo de B del campo; el segundo, de la variación del área de la espira; y el tercero, de la variación de la rotación angular de la espira respecto al campo magnético.
Apliquemos una semionda sinusoidal a un electroimán cuyo entrehierro sea una cuba electrolítica. La tensión inducida en cada partícula en movimiento será variable y será la suma debida al movimiento y a la frecuencia de la onda aplicada. Por lo tanto, dependerá en gran parte de la frecuencia aplicada. O bien una tensión variable a los electrodos en una cuba electrolítica; en ambos casos se producirá una tensión inducida cuyo valor vendrá dado por:
Fem . = d? / dt =
Fem. = d f · sen / dt = (entre 0 y p )
Fem. = f · cos (entre 0 y p )
Fem. = 1 / 2 · ? · ?m = 4,44· f· ?m
El valor eficaz nos da el valor de la Fem. inducida y que afecta a la movilidad de los iones.
Se puede enunciar que ciertas ondas electromagnéticas asociadas a un campo eléctrico aumentan la movilidad iónica en una disolución electrolítica.
La inducción magnética por sí sola no ejerce ningún desplazamiento de iones dentro de la disolución. Lo único es que se genera una Fem. en sentido transversal.
Además, se está estudiando el aspecto físico de forma teórica, pero la realidad es otra. Además del movimiento debido al campo eléctrico llamado de migración hay otros como el de difusión y el de convección.
Estudio de las ondas electromagnéticas
Han pasado unos años desde que se inventara el telégrafo y el teléfono por cable. Las comunicaciones tanto por radio, de V o la telefonía móvil es habitual en nuestros días. Las señales se transmiten por medio de ondas llamadas portadoras, bien modulada en amplitud o en frecuencia.
La frecuencia de las ondas portadoras están comprendidas entre 106 y 109 hercios, y si son alternas, los efectos electrolíticos son nulos: lo que avanzan en un semiperíodo, retroceden en el siguiente; pero no ocurre lo mismo si en vez de ser alternas pasan a ser variables y en ambos semiperíodos se suman esos valores. Se puede estar frente a un proceso electroquímico favorecido por inducción de alta frecuencia y afectar a las células vivas protegidas contra la intensidad de campo eléctrico E por la doble capa y favorecida, para bien o para mal, por el campo magnético asociado al campo eléctrico.
Las ondas portadoras, generadas en un circuito formado por una inductancia y un condensador, donde se produce un campo eléctrico variable E que a su vez crea un campo magnético siendo éstos perpendiculares entre sí y a la dirección de su propagación.
Su estudio está determinado por las ecuaciones de Maxwell, que no considero necesario desarrollar y que está fuera del alcance de este estudio.
Se puede diseñar una cuba electrolítica a cuyos electrodos se les aplique una tensión variable y a su vez atravesada perpendicularmente por un campo magnético variable de la misma frecuencia y en fase ambos campos. Comprobar los efectos producidos y compararlos con otros de intensidad de campo constante.
No se puede decir que las ondas de radiofrecuencia ionicen por radiación los cuerpos que están sometidos a dichas ondas; lo pueden hacer por conducción. Para que se produzca, deben darse ciertas circunstancias:
- El valor medio de las ondas debe tener un valor distinto de cero, lo que ocurre cuando las ondas están distorsionadas en amplitud. Dicha distorsión se puede producir al generar las ondas, en su transmisión o en el receptor.
- La intensidad de campo debe tener un valor mínimo que supere lo que se ha denominado fuerza contraelectromotriz en un proceso electrolítico y que en todo caso sea capaz de superar la tensión que se produce en la doble capa.
- El valor de la intensidad de campo se ve aumentado por la frecuencia; obsérvese que se induce una tensión que es proporcional a la variación del flujo y éste, a su vez, es proporcional a la frecuencia.
En la electrolisis lo fundamental es el proceso químico que se produce en cada electrodo; hasta ahora se ha considerado un solo ánodo y un solo cátodo, o en todo caso un electrodo más llamado patrón. Una cuba electrolítica con un ánodo y varios cátodos o viceversa, varios ánodos y un solo cátodo, con las condiciones anteriormente citadas se puede llegar a proceso químico elevado en un punto determinado cuando hay un solo electrodo y varios procesos químicos en los electrodos contrarios cuando son varios.
Electroquímica en las células
Los líquidos intracelulares y extracelulares de los organismos vivos contienen cantidades significativas de iones disueltos; para los mamíferos la molaridad es de 0,03 mol / litro.
Los principales iones son el Cl; Na+ ; K+ permeables a la membrana celular. Otros iones orgánicos tienen permeabilidad bastante baja.
Las células poseen una diferencia de potencial Vin-Vex comprendida entre -30 mV y -100 mV a través de su membrana, siendo el potencial inferior en el interior de la célula. En algunos casos, debido a un impulso o a una contracción, el valor se puede hacer positivo momentáneamente. El hecho de que haya una diferencia de potencial indica que hay una doble capa en la membrana de la célula; esta diferencia de potencial depende de las concentraciones de los iones Cl–; Na+ y K+ tanto en el interior como en el exterior de la célula y a la permeabilidad de la membrana a dichos iones. Goldman en 1943 utilizó una fórmula para relacionar las concentraciones y las permeabilidades de estos iones con la diferencia de potencial existente en una célula biológica.
Cuando no existe diferencia de potencial la célula está muerta.
Por lo tanto, la célula en un ser vivo se comporta como un proceso electrolítico. Determinadas ondas electromagnéticas de alta frecuencia pueden favorecer para bien o para mal dicho proceso y podría ser la ionización por conducción asociada a determinadas sustancias disueltas junto a la célula a tratar una nueva forma de neutralizar la diferencia de potencial celular. La tensión aplicada, su forma de onda, amplitud, frecuencia y tiempo empleado son constantes a considerar
Bibliografía
William D. Stevenson. Análisis de sistemas de potencia.
Marcelo Rodríguez Danta. Campos electromagnéticos.
Jacob Millman y Cristos Chalkior. Dispositivos y circuitos electrónicos.
Carlos Sánchez del Río. Física Quántica.
Robert M. Eisberg y Lawrence S. Lenner. Física: fundamentos y aplicaciones, vol II.